Vinblastin sulfat
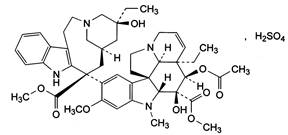 Vinblastini
sulfas
Vinblastini
sulfas
C46H58N4O9.
H2SO4
P.t.l: 909,0
Vinblastin
sulfat là methyl (3aR,4R,5S, 5aR,10bR,13aR)-4-(acetyloxy)-3a-ethyl-9
-[(5S,7R,9S)-5-ethyl-5-hydroxy-9-(methoxycarbonyl)-1,4,5,6,7,8,9,10-octahydro-2H-3,
7-methanoazacycloundecino[5,4-b]indol-9-yl
]-5-hydroxy-8-methoxy-6-methyl-3a,4,5,5a,6,11,12,13a-octahydro-1H-indolizino
[8,1-cd]carbazol-5-carboxylat sulfat, phải chứa từ 95,0
đến 104,0% C46H58N4O9. H2SO4,
tính theo chế phẩm đã làm khô.
Tính chất
Bột
kết tinh trắng hoặc hơi vàng nhạt, rất
dễ hút ẩm.
Dễ
tan trong nước, thực tế không tan trong ethanol 96%.
Định tính
A.
Phổ hồng ngoại (Phụ lục 4.2) của chế
phẩm phải phù hợp với phổ hồng ngoại
đối chiếu của vinblastin
sulfat chuẩn (ĐC).
B.
Trong phép thử “Định lượng”, pic chính trong
sắc ký đồ của dung dịch thử phải có
thời gian lưu tương ứng với thời gian
lưu của pic chính trong sắc ký đồ của dung
dịch đối chiếu (1).
Độ trong và màu sắc của dung dịch
Dung dịch S: Hoà tan
50,0 mg chế phẩm trong nước
không có carbon dioxyd (TT) và pha loãng thành 10,0 ml bằng cùng dung
môi.
Dung
dịch S phải trong (Phụ lục 9.2) và màu không
được đậm hơn màu mẫu V7
(Phụ lục 9.3, phương pháp 1).
pH
Pha
loãng 3 ml dung dịch S thành 10 ml bằng nước không có carbon dioxyd (TT), dung dịch thu
được phải có pH từ 3,5 đến 5,0
(Phụ lục 6.2).
Tạp chất liên quan
Trong
phép định lượng, trên sắc ký đồ
của dung dịch thử: diện tích của bất
kỳ pic phụ nào đều không được lớn
hơn diện tích của pic chính trên sắc ký đồ
của dung dịch đối chiếu (2) (2,0%); tổng diện tích của các pic
phụ không lớn hơn 2,5 lần diện tích của pic
chính trong sắc ký đồ của dung dịch đối
chiếu (2) (5,0%) và bỏ qua các pic có diện tích nhỏ
hơn diện tích của pic trong sắc ký đồ
của dung dịch đối chiếu (3).
Mất khối lượng do làm khô
Không
được quá 15,0% (Phụ lục 9.6).
(0,050
g; chân không; 105 °C; 2 giờ).
Định lượng
Định
lượng theo phương pháp sắc ký lỏng (Phụ
lục 5.3).
Pha động: Methanol
- dung dịch diethylamin 1,5% (tt/tt) đã được
điều chỉnh đến pH 7,5 bằng acid phosphoric -
acetonitril (50 : 38 : 12).
Dung dịch thử:
Pha loãng 1,0 ml dung dịch S thành 5,0 ml bằng nước.
Dung dịch đối chiếu (1): Hoà tan 5,0 mg vinblastin sulfat chuẩn
(ĐC) trong nước để
được 5,0 ml.
Dung dịch đối chiếu (2): Pha loãng 1,0 ml dung dịch đối
chiếu (1) thành 50,0 ml bằng nước.
Dung dịch đối chiếu (3): Pha loãng 1,0 ml dung dịch đối
chiếu (2) thành 20,0 ml bằng nước.
Dung dịch phân giải:
Hoà tan 1,0 mg vincristin sulfat chuẩn (ĐC) trong 1,0 ml dung dịch đối chiếu
(1).
Bảo
quản các dung dịch trên trong nước đá
trước khi dùng.
Điều kiện sắc ký:
Cột
thép không gỉ (25 cm x 4,6 mm) được nhồi pha
tĩnh B (5 mm) (zorbax C8 là thích hợp).
Cột
bảo vệ được nhồi silica gel thích hợp
nằm giữa buồng tiêm và cột phân tích.
Detector
quang phổ hấp thụ tử ngoại ở
bước sóng 262 nm.
Tốc
độ dòng: 1 ml/phút.
Thể
tích tiêm: 10 ml.
Cách tiến hành:
Tiêm
mỗi dung dịch trên và ghi sắc ký đồ cho
đến thời gian gấp 3 lần thời gian lưu
của pic tương ứng với vinblastin.
Phép
thử chỉ có giá trị khi hệ số phân giải
giữa các pic tương ứng với vincristin và vinblastin
trong sắc ký đồ của dung dịch phân giải ít
nhất là 4 và tỷ số giữa tín hiệu và nhiễu
đường nền của pic trên sắc ký đồ
của dung dịch đối chiếu (3) ít nhất là 5.
Tính
hàm lượng phần trăm của C46H58N4O9.
H2SO4 dựa theo diện tích của pic chính
của dung dịch thử và dung dịch đối
chiếu (1) và hàm lượng của vinblastin sulfat
chuẩn.
Độ vô khuẩn
Nếu
chế phẩm dự định dùng để sản
xuất thuốc tiêm phân liều mà không tiến hành tiệt
khuẩn nữa thì phải đáp ứng phép thử này
(Phụ lục 13.7).
Bảo quản
Đựng trong bình
thuỷ tinh kín, tránh ánh sáng và bảo quản ở nhiệt
độ không quá -20 °C. Nếu chế phẩm
là vô khuẩn thì phải đựng trong bình thuỷ tinh vô
khuẩn, đậy thật kín để tránh nhiễm vi
khuẩn. Trên nhãn cần ghi rõ
chế phẩm là vô khuẩn hay không.
Loại thuốc
Chống ung thư.
Chế
phẩm
Thuốc tiêm.